2026-03-06 15:44:19 by admin  119
119
 导读:在上一篇中,我们讨论了颈动脉粥样硬化性疾病(CarAD)的流行病学与病理生理基础。本篇继续系统梳理CarAD的临床表现、影像学评估与卒中风险。简要翻译如下(原文链接:https://pubmed.ncbi.nlm.nih.gov/37632337/):
导读:在上一篇中,我们讨论了颈动脉粥样硬化性疾病(CarAD)的流行病学与病理生理基础。本篇继续系统梳理CarAD的临床表现、影像学评估与卒中风险。简要翻译如下(原文链接:https://pubmed.ncbi.nlm.nih.gov/37632337/):
四. 颈动脉粥样硬化性疾病(CarAD) 的临床表现无症状动脉粥样硬化性颈动脉狭窄(asymptomatic carotid stenosis,AsxCS)指从未引起神经系统症状的颈动脉病变。常用的定义是:不存在与该侧颈动脉相关的、近期发生的(通常指 <6 个月,但“有症状”的时间界值在不同研究中可为 1–12 个月,甚至更久远)同侧卒中、短暂性脑缺血(TIA)发作或短暂性单眼失明。需要指出的是,既往发生过对侧或后循环卒中/TIA 的患者,以及在横断面脑影像学检查显示无症状脑梗死,或存在同侧颈动脉狭窄的视网膜栓塞患者(如在糖尿病视网膜病变筛查中发现),尽管已有明确的脑梗死证据,传统上仍被归类为“无症状”人群。因此,AsxCS 人群实际上涵盖了范围广泛的患者,其中部分患者的卒中风险明显更高。这种人群异质性也反映在 AsxCS 的临床研究中:卒中风险较高的患者更倾向于接受介入性治疗,因此较少被纳入单纯药物治疗的观察性研究或比较单纯药物治疗与颈动脉手术/支架治疗的随机对照试验;相反,卒中风险较低的患者则不太可能被随机分配至比较两种侵入性治疗方式的试验中。在解读临床试验结果并制定治疗策略时,必须充分考虑这一重要但易被忽视的差异。
2. 症状性狭窄
CarAD 所致症状大多源于斑块炎症和破裂,继而局部形成的血栓或斑块碎片发生栓塞,阻塞视网膜或脑动脉,最常见于前循环。在高度狭窄或闭塞的情况下,颈动脉相关的脑缺血亦可由血流减少(血流动力学机制)所致。由脑缺血引起、持续时间 <24 小时(更常见 <60 分钟)的局灶性神经功能缺损称为 TIA,而缺血性卒中的临床定义通常指症状持续 >24 小时。局灶性神经功能症状可能单独出现,也可能组合出现,包括运动障碍(例如仅手、臂、面部或腿的轻瘫)、感觉缺损、失语、半侧忽略(指大脑一侧受损后,患者对身体另一侧或空间的感知与注意力缺失)以及偏盲。另一种被认可的卒中机制是闭塞颈动脉的血栓延伸,可表现为症状在数小时至数日内逐渐加重;同时伴随血流动力学受损,导致脑灌注减少,并可能出现阳性运动现象,即所谓“肢体抖动型 TIA”。
涉及ICA或眼动脉的颈动脉狭窄可导致多种眼部表现:
视网膜动脉闭塞或栓塞,可能无临床症状,也可能表现为眼部症状。
短暂性单眼视力丧失(黑矇)和眼卒中是常见表现形式,
其他慢性眼部症状(如眼部缺血综合征)也应促使患者接受颈动脉超声检查或替代性颈动脉影像学检查。
准确评估狭窄程度至关重要,狭窄程度仍是各大指南认可的、决定患者管理策略的核心参数。对于无症状患者,当狭窄程度超过 60–70% 时才考虑介入治疗;而在有症状患者中,介入治疗的阈值为 >50%,且复发性卒中风险随狭窄程度增加而急剧上升。双功能超声(DUS)检查是狭窄程度首选筛查手段,具有成本低、无创且安全的优点。横断面血管造影,包括 CT 血管成像(CTA)或磁共振血管成像(MRA),是 DUS 的重要替代或补充手段,并可同时评估脑循环。DUS 在识别颈动脉狭窄方面有效,但在精确判断中至重度狭窄程度方面,其准确性较差。近期对 338 家经认证的 DUS 实验室中超过 33000 例检查记录的分析显示,患者是否被判定为中度狭窄并进入随访监测,或是否被认定为重度狭窄并成为血运重建候选者,很大程度上取决于超声检查所在的中心。此外,研究表明,仅依赖 DUS 评估狭窄程度时,大约每 6 条动脉中就有 1 条会在 CTA 复查后被重新分级,这提示治疗决策不应仅基于 DUS。充分认识颈动脉 DUS 检查中的常见成像陷阱,有助于避免误判。因此,尽管 DUS 仍是发现颈动脉狭窄的一线检查手段,2017 年 ESC 指南仍建议在任何介入治疗前使用 CTA(或 MRA)评估狭窄程度。狭窄程度通常采用北美有症状性颈动脉内膜剥脱术试验(NASCET)方法进行评估,即以狭窄远端的“正常”血管直径作为参照,与狭窄最窄处直径比较,并以直径狭窄百分比表示。狭窄程度也可通过 CTA 和/或 MRA 测量,且常以面积狭窄百分比而非直径狭窄百分比表示。由于面积计算遵循 π × (d/2)² 的公式,直径狭窄与面积狭窄之间呈非线性关系:在同心性管腔缩小的情况下,75% 面积狭窄相当于 50% 直径狭窄,而 75% 直径狭窄则对应 94% 面积狭窄。部分临床试验采用单一影像学方法作为狭窄程度的入组标准,另一些则根据所用影像学方式设定不同阈值,或制定了详细的狭窄程度验证算法。由于不同影像学手段和测量方法会影响管理决策,临床医生在将试验结果应用于具体患者时,应仔细参考各试验中采用的狭窄测量方法。鉴于测量结果的临床相关性,未来指南中或需对不同影像学方式下的“狭窄百分比”测量方法进行统一和校正。除狭窄程度外,颈动脉斑块的形态和成分同样会影响卒中风险。目前可采用多种无创及有创影像学技术,包括超声、CT、MRI以及PET。颈动脉斑块易损性的影像学特征包括:斑块体积或颈动脉壁厚度增加、炎症活动增强、新生血管形成、斑块内出血(IPH)、溃疡及内皮糜烂、富脂质坏死核心(LRNC)、纤维帽破裂,以及微气泡和血流紊乱。这些提示斑块高风险的特征往往相互关联。例如,在前瞻性颈动脉多模态影像预后研究(CAMP)中,对无症状、单侧中度颈动脉狭窄患者进行分析发现,CTA 上的斑块溃疡在校正狭窄程度后,仍与 IPH 或 LRNC 的存在显著关联(OR 4.2,95% CI 1.3–13.2;OR 4.0,95% CI 1.4–11.2)。此外,在存在亚临床脑栓塞性梗死的患者中,LRNC 的发生率更高(50% vs. 17%,P ≤ 0.05)。同时,合并 IPH 或 LRNC 的患者在标准化认知功能测试中的表现显著较差(评分 1.6 ± 1.1 vs. 2.2 ± 1.4,P < 0.05)。¹⁸F-FDG PET 可在约 30% 的颈动脉粥样硬化病变中显示炎症活动。近期对 14 篇文献(539 例患者)的系统评价与荟萃分析表明,¹⁸F-FDG PET 检测到的颈动脉斑块炎症是有症状性疾病的重要标志。除作为动脉粥样硬化活动性的指标外,¹⁸F-FDG PET 还可作为抗炎治疗疗效的替代终点。三时间点的 ¹⁸F-FDG PET 成像研究显示,即使在 3 个月时血浆 LDL-C 已稳定降至目标以下,他汀的抗炎作用仍可持续至 1 年。对 11 个队列(共 290 例)进行的荟萃分析发现,与无症状动脉相比,近期发生脑缺血事件同侧的颈动脉 ¹⁸F-FDG 摄取显著升高(Cohen’s d = 0.492;CI 0.130–0.855;P = 0.008),且与狭窄程度无关,提示 ¹⁸F-FDG PET 可能在临床决策中发挥辅助作用。事实上,¹⁸F-FDG PET 还有助于在隐源性缺血性卒中中识别责任颈动脉斑块。就临床可行性而言,MRI 检测到的 IPH 目前被认为是同侧缺血性卒中最重要的无创危险因素[有症状患者的风险比(HR)为 10.2,95% CI 4.6–22.5;无症状个体 HR 为 7.9,95% CI 1.3–47.6]。最新研究显示,纤维帽变薄或破裂与卒中风险的关联强于狭窄程度本身。此外,近期研究还发现,在轻至中度颈动脉狭窄患者中,总斑块体积是同侧缺血性卒中或 TIA 复发的独立危险因素。为改善不同影像学技术(如超声、CT、MRI)下对颈动脉斑块成分和形态的报告质量,并促进患者管理(包括治疗方式选择)以及放射科医师、临床医生与科研人员之间的沟通,提出了一种新的标准化报告体系——斑块报告与数据系统(Plaque-Reporting and Data System,Plaque-RADS)。结合狭窄程度与斑块形态学评估的算法,未来很可能在颈动脉血运重建的临床决策中发挥越来越重要的作用。一项前瞻性研究在 30 天内发生颈动脉相关非重度卒中(改良 Rankin 评分 ≤3)或 TIA 的患者中,评估早期复发性卒中预测(推导队列 109 例,验证队列 87 例),结果提示,将狭窄程度(CTA,NASCET 方法)与炎症(¹⁸F-FDG 摄取)相结合的策略,可能有助于在当前获益尚不明确的人群中,更好地筛选适合进行颈动脉血运重建的患者,但仍需在更低风险人群中开展大规模研究加以验证。检测近期脑缺血最敏感的方法是弥散加权磁共振成像(DWI),该技术可在缺血发生后数分钟内显示潜在可逆的细胞能量衰竭及早期细胞毒性水肿(细胞肿胀)区域的高信号。颈动脉疾病所致栓塞性卒中的典型影像表现为:位于大脑中动脉(MCA)供血区以及大脑中、前、后动脉交界区的多发小皮质梗死灶。即使患者仅表现为短暂症状且无持续性神经功能缺损(即临床TIA),DWI/FLAIR仍可发现脑组织梗死。近期一项纳入633例TIA患者的研究显示,DWI阳性与TIA后10年内复发缺血性卒中的风险显著升高相关(HR 2.66,95% CI 1.28–5.54,P = 0.009)。TIA是一种脑部紧急状态,应尽快进行评估,包括脑部影像及颈动脉影像学检查,并针对TIA的病因进行治疗,以预防卒中发生。英国国家卫生与临床优化研究所(NICE)近期建议:所有疑似卒中或TIA患者均应在当天完成MRI检查(包括DWI和FLAIR序列)以及颈动脉影像学检查(颈动脉双工超声或CTA/MRA)。临床无症状性脑梗死是指在无急性神经功能障碍病史的情况下,通过影像学或神经病理学发现脑梗死证据。与对侧大脑半球相比,临床无症状性CarAD患者在狭窄上游区域更常见隐匿性脑梗死。与既往TIA类似,影像学发现的无症状脑梗死可使未来卒中风险增加约2倍。因此,对于存在影像学证实但临床无症状脑梗死的CarAD患者,可根据有症状病变的狭窄程度阈值考虑血运重建治疗。卒中的新定义为:“基于神经病理学、神经影像学和/或临床证据,由缺血导致的细胞死亡”。根据这一逐渐被采纳的定义,即便相关症状仅为短暂性,只要DWI/FLAIR显示脑梗死,即可诊断为卒中。 在当代临床试验的纳入标准和终点指标中,脑卒中的组织学(脑梗死)定义正日益与传统的(临床)脑卒中定义相结合。对于栓塞性卒中,影像学血栓分析正被用于探索病因。卒中仍是全球范围内致死致残的主要原因之一。然而,在过去20年中,“三联药物治疗”的改进(尤其是他汀类药物的广泛应用)可能降低了颈动脉狭窄的自然卒中风险。随机研究证据表明,他汀可有效稳定易损性颈动脉斑块。在心脏保护研究(Heart Protection Study)中,使用40 mg辛伐他汀使CEA发生率降低了一半(0.4% vs. 0.8%,P = 0.0003)。在明确为动脉粥样硬化性卒中或TIA的患者中,将LDL-C控制在<70 mg/dL,可每治疗30人避免1例重大血管事件。对864例至少一侧≥50%无症状颈动脉狭窄(男性51.5%)且至少接受3次随访超声检查的患者分析显示:未使用或仅使用低强度他汀、血压控制不佳以及狭窄程度进展是缺血性卒中或TIA复合终点的独立预测因素(平均随访6.5 ± 3年)。卒中风险呈连续梯度分布:从完全无症状人群的极低风险(<1%/年),到虽无症状但存在易损斑块特征者的中等风险,再到近期发生同侧神经系统事件患者的高风险(>10%/年)。值得注意的是,尽管普通狭窄性CarAD人群的“平均”卒中风险约为1%/年,但在临床表现为心血管疾病或糖尿病的患者中风险显著升高(高达每年2.5%),而具有临床或影像学证据表明既往存在脑梗死的患者风险则更高。卒中风险具有累积性,因此颈动脉相关卒中的“平均统计学”10年风险介于10%至25%之间。
在CarAS患者中,卒中家族史是重要危险因素。一项纳入864例CarAS患者(年龄72±8岁;男性68%)和1698例对照者(年龄61±11岁;男性55%)的队列研究显示,接受无创血管检测的患者中,CarAS组卒中家族史发生率显著高于对照组(OR = 2.02,95% CI:1.61–2.53)。即使仅考虑65岁前卒中事件,经年龄、性别、体重指数、吸烟、糖尿病、高血压及血脂异常校正后,该关联仍保持显著(OR = 1.41,95% CI:1.06–1.90)。对极低风险患者实施颈动脉介入治疗的风险缺乏合理性依据,关键在于识别出那些尽管接受三联药物治疗(抗血小板药物、他汀类药物、降压药)仍存在卒中风险增加的显著颈动脉狭窄患者亚群,这些患者可能从颈动脉手术或支架置入中获得显著获益。此外,近期一项针对接受神经血栓切除装置治疗的急性缺血性卒中患者的系统评价表明,非狭窄性颈动脉斑块与隐源性卒中存在显著关联,提示‘非显著性’病变在病因未明的栓塞性卒中中可能具有潜在机制作用。学界日益认识到‘非狭窄性’颈动脉斑块可能是脑栓塞的重要来源。当存在高风险斑块特征时,非狭窄性颈动脉斑块导致卒中/短暂性脑缺血发作(TIA)复发的风险尤为不可忽视,该风险从2.6/100人年增至4.9/100人年。最新系统综述现有证据表明,对狭窄程度≤50%的症状性颈动脉疾病实施血运重建术可能是预防卒中复发的潜在有益策略。
大多数严重卒中发作时并无临床预警症状。因此,一线采用强化药物治疗作为一级预防至关重要。然而,尽管AsxCS患者严格遵循药物治疗方案,仍有相当比例患者依然发生神经事件。值得注意的是,目前尚无前瞻性验证的卒中风险量化工具可用于AsxCS受试者。
(未完待续,下一篇解读将进一步聚焦:颈动脉疾病的治疗, 包括药物、手术和支架等)
![]() 119
119  导读:在上一篇中,我们讨论了颈动脉粥样硬化性疾病(CarAD)的流行病学与病理生理基础。本篇继续系统梳理CarAD的临床表现、影像学评估与卒中风险。简要翻译如下(原文链接:https://pubmed.ncbi.nlm.nih.gov/37632337/):
导读:在上一篇中,我们讨论了颈动脉粥样硬化性疾病(CarAD)的流行病学与病理生理基础。本篇继续系统梳理CarAD的临床表现、影像学评估与卒中风险。简要翻译如下(原文链接:https://pubmed.ncbi.nlm.nih.gov/37632337/):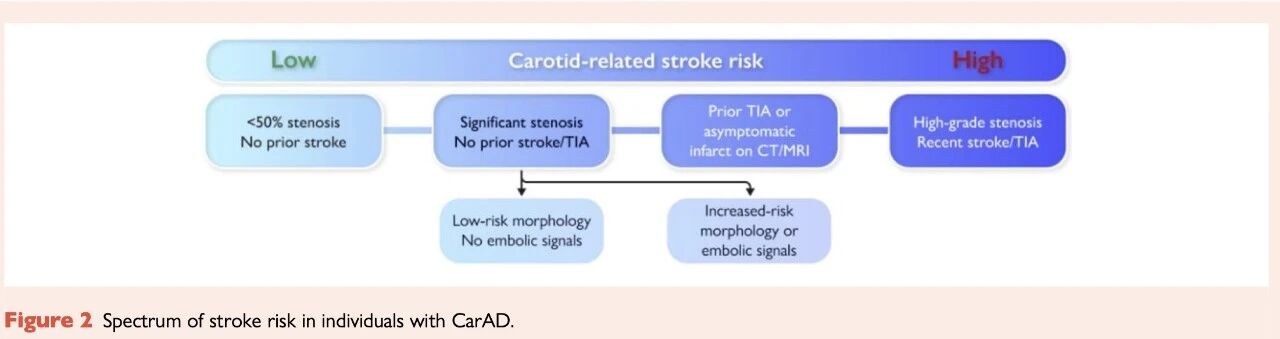

 京公网安备 11010502042883号
京公网安备 11010502042883号